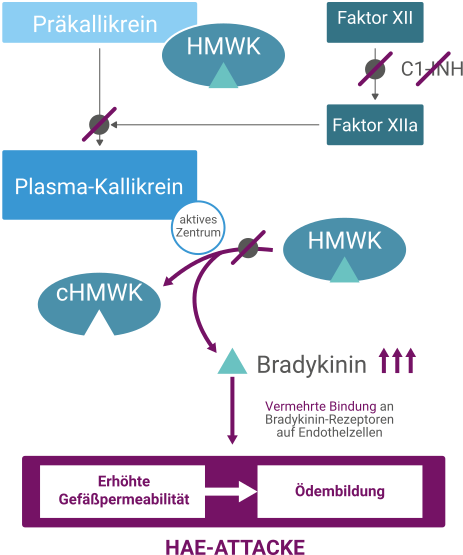
In der Pathophysiologie des Hereditären Angioödems (HAE) steht die unzureichende Kontrolle des sogenannten Kallikrein-Kinin-Systems durch den C1-Inhibitor (C1-INH) im Mittelpunkt. Dadurch ist dieses System während einer HAE-Attacke übermäßig aktiv. Das Resultat ist eine vermehrte Produktion von Bradykinin. Dieses Peptidhormon steht am Ende der Kaskade und vermittelt Reaktionen, die zu einer Vasodilatation und erhöhter vaskulärer Permeabilität führen. Infolgedessen kommt es bei einem Überangebot von Bradykinin zu einem Flüssigkeitsaustritt in das Gewebe – ein Ödem entsteht.1,2
Weitere Faktoren, die im Kallikrein-Kinin-System eine Rolle spielen, sind der Gerinnungsfaktor XII, der am Anfang der Signal-Kaskade steht, und der Faktor XIIa, der aus ihm entsteht und Präkallikrein in aktives Plasma-Kallikrein umwandelt. Dieses ist wiederum der Haupttreiber der Freisetzung von Bradykinin aus dem hochmolekularen Kininogen (HMWK). In diesem System hemmt der C1-INH den Faktor XIIa sowie das Plasma-Kallikrein. Durch seine Aktivität wird die Freisetzung von Bradykinin im Normalfall auf ein physiologisches Niveau beschränkt.3-6
Beim C1-INH handelt es sich um einen Serin-Protease-Inhibitor (Serpin), der in Hepatozyten, Fibroblasten, Monozyten, Makrophagen und Endothelzellen gebildet wird. Auch in der Komplementkaskade, der Fibrinolyse sowie der Gerinnungskaskade hat der C1-INH eine physiologische Rolle. Dort kommt es aber bei HAE-Patienten zu keinerlei negativen Effekten.3,4,5